[Chăn nuôi Việt Nam] – Nghiên cứu được thực hiện nhằm đánh giá tỷ lệ lưu hành và sự hiện diện các gen kháng kháng sinh của Salmonella spp. tại các trang trại nuôi vịt ở Đồng bằng sông Cửu Long. Tổng cộng 428 mẫu được thu thập từ 4 tỉnh: Hậu Giang, Sóc Trăng, Tiền Giang và Vĩnh Long và phân tích bằng kỹ thuật Multiplex-PCR.
Kết quả cho thấy Salmonella spp. hiện diện trong 187/428 mẫu (43,7%), với tỷ lệ cao nhất tại Sóc Trăng (52,0%) và thấp nhất tại Hậu Giang (32,0%) (P<0,05). Trong số 186 mẫu dương tính, các gen kháng thuốc phổ biến nhất là gyrA, dfrA1 và tetA (26,9%), tiếp đến là aac(3)–IV (17,7%), sul1 (14,5%) và blaTEM (4,3%).
Đáng chú ý, Vĩnh Long ghi nhận tỷ lệ hiện diện gen cao nhất, cho thấy nguy cơ cục bộ liên quan đến việc sử dụng kháng sinh. Xét theo loại mẫu, nước thải có tỷ lệ phát hiện Salmonella spp. cao nhất (53,4%), kế đến là mẫu swab (43,0%) và phân môi trường (35,6%) (P <0,05). Sự phân bố gen kháng thuốc cũng khác biệt theo loại mẫu: gyrA và aac(3)–IV chiếm ưu thế trong swab; dfrA1, tetA và sul1 phổ biến trong phân môi trường; trong khi blaTEM ít gặp nhất ở cả ba nhóm mẫu. Kết quả này khẳng định nước thải và môi trường chuồng trại là những ổ chứa quan trọng của Salmonella kháng kháng sinh (KKS), đồng thời nhấn mạnh sự cần thiết của công tác giám sát và quản lý sử dụng kháng sinh trong chăn nuôi vịt.
VẬT LIỆU VÀ PHƯƠNG PHÁP NGHIÊN CỨU
Đối tượng, địa điểm và thời gian Vi khuẩn Salmonella spp.
Trên các trại vịt nuôi ở 4 tỉnh Hậu Giang, Sóc Trăng, Tiền Giang và Vĩnh Long của Đồng bằng sông Cửu Long được lấy mẫu từ tháng 8/2024 đến tháng 12/2024 và phân tích tại phòng thí nghiệm Đại học Cần Thơ.
Phương pháp
Nội dung 1: Khảo sát tỷ lệ nhiễm vi khuẩn Salmonella spp. trên vịt tại địa bàn nghiên cứu
Phương pháp lấy mẫu: Tại mỗi hộ chăn nuôi, phỏng vấn bằng bảng câu hỏi để thu thập các thông tin dùng cho phân tích dịch tễ và thu 10 mẫu swab, 10 mẫu môi trường (5 mẫu phân nền chuồng, 5 mẫu nước thải).
Mẫu swab: Lấy từ phân hoặc dịch hậu môn của vịt bằng tăm bông vô trùng, bảo quản trong ống Falcon vô trùng, đặt trong thùng đá khô và chuyển về phòng thí nghiệm trong vòng 24 giờ. Mẫu phân nền chuồng: Thu 5 mẫu tại các vị trí khác nhau trong nền chuồng bằng tăm bông vô trùng, bảo quản tương tự.
Mẫu nước thải: Thu 5 mẫu (20ml/mẫu) từ các vị trí hồ tắm, nước uống, nước đọng nền chuồng bằng ống Falcon 50ml vô trùng, bảo quản trong thùng đá khô và phân tích trong vòng 24 giờ.
Phương pháp xác định mẫu dương tính với S. enteritidis và S. Pullorum: Việc xác định mẫu dương tính được thực hiện bằng kỹ thuật Multiplex-PCR với hai cặp mồi trường và mẫu nước thải được vận chuyển đến phòng thí nghiệm và tăng sinh trong 24 giờ. Chiết xuất DNA tuân theo hướng dẫn của nhà sản xuất TopPURE® Genomic DNA Extraction Kit (Giải pháp sinh học ABT, Việt Nam).
Xét nghiệm Multiplex-PCR được tiến hành nhằm phát hiện đồng thời S. pullorum và S. enteritidis. Cặp mồi SPS4_00301–SPS4_00311 GCACGCGACGTTCAAATCTG_F; GACGGTCACACCAAATAAGC_R) được sử dụng để phát hiện S. pullorum và cặp mồi CitE2 (TCGACATCGCCACCTCCAG_F; CGGCAATCACCTCATACAT_R) phát hiện S. enteritidis, nhắm vào gen 16S rRNA theo khuyến nghị của Liu và ctv (2022). Thành phần phản ứng Multiplex-PCR để xác định S. enteritidis và S. pullorum (gen 16S rRNA) bao gồm hỗn hợp MyTaq (10,0µl), mồi xuôi (10µM) (0,75µl), mồi ngược (10µM) (0,75µl), mẫu DNA (3,0µl) và nước đạt chuẩn PCR (4µl). Các ống phản ứng được đặt trong máy chu trình nhiệt với chương trình sau: 1 chu kỳ ở 950 C trong 5 phút, tiếp theo là 30 chu kỳ ở 950 C trong 40 giây, 580 C trong 30 giây và 720 C trong 30 giây, kết thúc bằng 1 chu kỳ ở 720 C trong 10 phút.
Nội dung 2: Xác định khả năng đề kháng kháng sinh của Salmonella spp. trên vịt
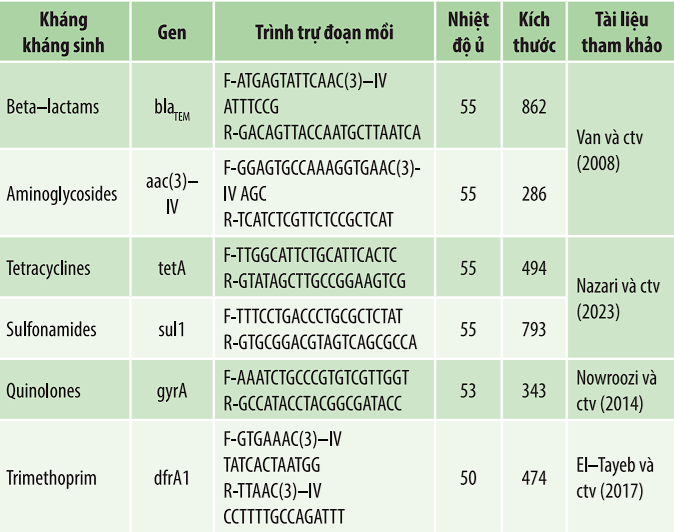
Khả năng đề kháng kháng sinh của các chủng Salmonella spp. được đánh giá thông qua sự hiện diện của một số gen KKS phổ biến tại khu vực ĐBSCL. Các mẫu DNA dương tính với cặp mồi định danh S. enteritidis và S. pullorum (SPS4_00301–SPS4_00311 và CitE2) được sử dụng để khảo sát các gen đề kháng, với trình tự mồi được trình bày ở bảng 1.
Bảng 1. Trình tự nucleotide của cặp mồi sử dụng trong phát hiện gen kháng kháng sinh của Salmonella spp.
Xử lý số liệu
Dữ liệu được nhập và xử lý bằng Microsoft Excel 2016. Các tham số thống kê cơ bản được phân tích bằng phần mềm Minitab v22.0. So sánh giữa các nhóm được thực hiện bằng Chi–square test (χ²) và Fisher’s exact test (áp dụng khi có ít nhất một tần suất lý thuyết <5).
KẾT QUẢ VÀ THẢO LUẬN
Tỷ lệ lưu hành vi khuẩn Salmonela spp.
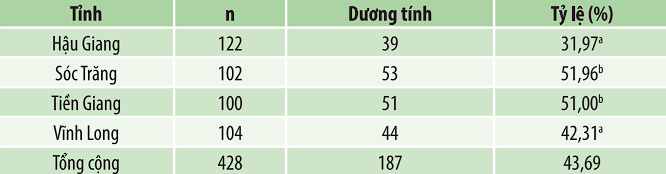
Kết quả về sự hiện diện của Salmonella spp. trên vịt từ các hộ chăn nuôi 4 tỉnh được trình bày ở bảng 2 cho thấy, trong tổng số 428 mẫu Salmonella spp. hiện diện 187 mẫu (43,69%). Tỉnh Sóc Trăng có cao nhất (51,96%; 53/102 mẫu) và Hậu Giang thấp nhất (31,97%; 39/122 mẫu) với sự khác biệt có ý nghĩa thống kê giữa các tỉnh (P <0,05). Điều này phản ánh sự phân bố không đồng đều của Salmonella spp. trong các tỉnh. Trong các nghiên cứu trước đây tại khu cực Đồng bằng sông Cửu Long, Tran và ctv (2004) phân lập được Salmonella spp. từ 7,1% tổng số mẫu ở lợn, gà và vịt. Tương tự, Tu và ctv (2015) ghi nhận tỷ lệ nhiễm rất cao ở các trang trại gà (64,7%), vịt (94,3%) và lợn (91,3%). Sự khác biệt giữa các nghiên cứu và giữa các tỉnh có thể do điều kiệnchăn nuôi, vệ sinh chuồng trại, mật độ đàn, mùa vụ và hiệu quả kiểm soát dịch bệnh. Theo EFSA (2019), mật độ nuôi cao và stress đàn làm tăng nguy cơ nhiễm Salmonella; trong khi Hoàng Thị Anh Phương và Lương Đoàn Minh Châu (2022) cũng cho thấy tỷ lệ nhiễm ở vịt có thể chịu ảnh hưởng bởi yếu tố mùa vụ.
Bảng 2. Lưu hành Salmonella spp. ở trại vịt
Ghi chú: Các giá trị trung bình mang các chữ cái khác nhau trong cùng cột là sự sai khác có ý nghĩa thống kê (P<0,05).
Theo từng loại mẫu
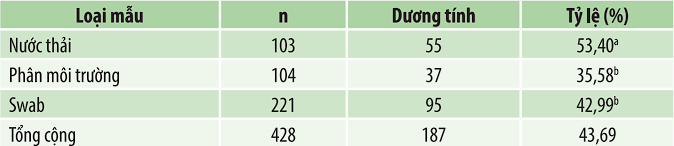
Kết quả về tỷ lệ lưu hành của Salmonella spp. ở các trang trại nuôi vịt theo từng loại mẫu được trình bày trong bảng 3 cho thấy, tỷ lệ dương tính cao nhất được ghi nhận ở mẫu nước thải là 53,40% (55/103 mẫu), tiếp theo là mẫu Swab với 42,99% (95/221 mẫu), và thấp nhất được ghi nhận ở mẫu phân môi trường với 35,58% (37/104 mẫu). Phân tích thống kê cho thấy có sự khác biệt có ý nghĩa về tỷ lệ phát hiện Salmonella spp. giữa các loại mẫu (P <0,05). Trong đó, mẫu nước thải ghi nhận tỷ lệ dương tính cao nhất, phản ánh vai trò quan trọng của môi trường nước như nguồn tồn lưu và phát tán Salmonella spp. trong chăn nuôi. Kết quả này khác biệt với một số nghiên cứu trước đây, Osman và ctv (2021) tại Malaysia ghi nhận tỷ lệ nhiễm cao hơn ở mẫu phân (59,5%) và Swab (46,3%) so với mẫu nước thải (35,7%).
Trong khi đó, Syed Abu Thahir và ctv (2023) báo cáo tỷ lệ nhiễm 45% ở đất và 30% ở nước thải. Tương tự, Saengthongpinit và ctv (2015) cũng ghi nhận tỷ lệ nhiễm ở nước (47,1%) cao hơn so với Swab (10,7%). Những khác biệt này có thể do đặc điểm môi trường, tính chất mẫu và điều kiện chăn nuôi khác nhau.
Bảng 3. Lưu hành Salmonella spp. ở trại vịt
Sự hiện của các gen kháng kháng sinh
Theo địa bàn khảo sát
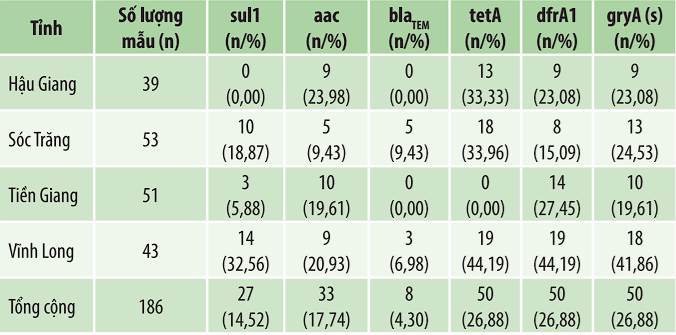
Kết quả về sự hiện diện của các gen KKS ở Salmonella spp. phân lập từ mẫu vịt tại các hộ chăn nuôi ở Đồng bằng sông Cửu Long được trình bày trong bảng 4 cho thấy, tổng số 186 mẫu dương tính với Salmonella spp., chỉ có 1 mẫu âm tính với cả 6 gen KKS khảo sát. Kết quả cho thấy, 3 gen được phát hiện phổ biến nhất là gyrA, dfrA1 và tetA với cùng tỷ lệ 26,88% (50/186 mẫu), tiếp theo là aac(3)–IV (17,74%; 33/186 mẫu) và sul1 (14,52%; 27/186 mẫu), trong khi blaTEM có tỷ lệ thấp nhất 4,30% (8/186 mẫu).
Phân tích theo tỉnh cho thấy sự khác biệt đáng kể: Vĩnh Long ghi nhận tỷ lệ cao nhất đối với hầu hết các gen (gyrA, dfrA1, tetA, sul1), Sóc Trăng nổi bật với tetA (33,96%) và blaTEM (9,43%), Hậu Giang có tỷ lệ cao với tetA (33,33%) và aac(3)–IV (23,98%) nhưng không phát hiện sul1 và blaTEM, trong khi Tiền Giang không ghi nhận tetA và blaTEM nhưng có mức dương tính trung bình với dfrA1 (27,45%) và aac(3)–IV (19,61%). Nhìn chung, Vĩnh Long là địa phương có mức độ hiện diện gen KKS cao nhất, phản ánh sự khác biệt trong điều kiện chăn nuôi và thực hành sử dụng kháng sinh, đồng thời cho thấy nguy cơ lan rộng các chủng Salmonella spp. kháng thuốc tại khu vực này.
Bảng 4. Tỷ lệ gen kháng kháng sinh theo tỉnh
Theo từng loại mẫu
Để đánh giá vai trò của từng loại mẫu trong duy trì và phát tán các chủng Salmonella spp. KKS, tỷ lệ xuất hiện của các gen KKS theo loại mẫu (nước thải, phân môi trường, tăm bông hậu môn) được khảo sát và trình bày trong bảng 5.
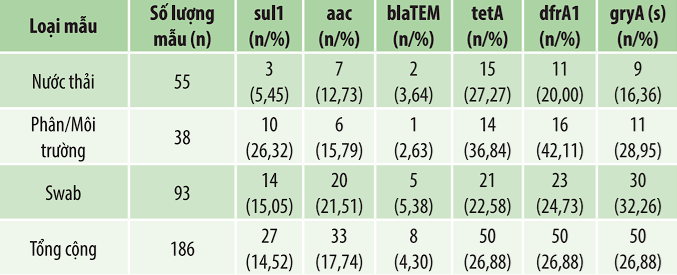
Bảng 5. Tỷ lệ gen kháng kháng sinh theo loại mẫu
Kết quả phân tích theo loại mẫu cho thấy, tỷ lệ phát hiện cao nhất thuộc về các gen gyrA, tetA và dfrA1. Cụ thể, gyrA phổ biến nhất trong mẫu swab (32,26%), tiếp theo là phân môi trường (28,95%) và thấp nhất ở nước thải (16,36%); dfrA1 được phát hiện nhiều trong phân môi trường (42,11%), sau đó là swab (24,73%) và nước thải (20,00%); tetA cũng chiếm tỷ lệ cao trong phân môi trường (36,84%), tiếp theo là nước thải (27,27%) và Swab (22,58%). Trong khi đó, sul1 phổ biến nhất ở phân môi trường (26,32%), aac(3)–IV cao nhất ở swab (21,51%) và blaTEM có tỷ lệ thấp nhất ở tất cả các loại mẫu (2,63–5,38%).
Sự khác biệt này phản ánh vai trò sinh học và môi trường của từng loại mẫu: swab phản ánh vi khuẩn sống tích cực trong đường ruột nên thường có tỷ lệ gen kháng cao, đặc biệt là gyrA và tetA liên quan đến nhóm quinolon và tetracycline vốn được sử dụng phổ biến trong chăn nuôi (Yang và ctv, 2019; Young và ctv, 2022). Phân môi trường là nơi tích tụ vi khuẩn từ nhiều cá thể, tạo điều kiện cho gen kháng như sul1 và dfrA1 duy trì và lan truyền nhờ plasmid và integron lớp 1 (Williamson và ctv, 2018; Urban-Chmiel và ctv, 2022). Ngược lại, nước thải có tỷ lệ phát hiện thấp nhất do sự pha loãng, cạnh tranh sinh học và tác động bất lợi từ môi trường, làm giảm khả năng sống sót của vi khuẩn mang gen kháng.
KẾT LUẬN
Kết quả nghiên cứu cho thấy, Salmonella spp. lưu hành với tỷ lệ cao trên đàn vịt tại các tỉnh Đồng bằng sông Cửu Long, với sự khác biệt đáng kể giữa các tỉnh và loại mẫu. Nước thải và phân môi trường được xác định là nguồn lưu giữ và phát tán quan trọng của Salmonella spp., trong khi sự hiện diện phổ biến của các gen kháng thuốc như gyrA, dfrA1 và tetA phản ánh mức độ sử dụng kháng sinh trong chăn nuôi vịt. Đặc biệt, tỉnh Vĩnh Long được ghi nhận có nguy cơ cao nhất liên quan đến sự lan rộng của Salmonella kháng thuốc.
Những kết quả này nhấn mạnh tính cấp thiết của việc tăng cường giám sát định kỳ, cải thiện vệ sinh môi trường chăn nuôi và quản lý sử dụng kháng sinh hợp lý. Đồng thời, nghiên cứu cung cấp cơ sở khoa học quan trọng phục vụ xây dựng chiến lược kiểm soát Salmonella spp. và hạn chế sự phát tán các gen KKS trong chăn nuôi vịt tại khu vực Đồng bằng sông Cửu Long.
Tài liệu tham khảo theo yêu cầu
Lâm Thị Ngọc Trang, Đỗ Ngọc Yến Phương, Nguyễn Vũ Thụy Hồng Loan (Trường Đại học Công nghệ TP. Hồ Chí Minh)
Nguyễn Trọng Ngữ (Đại học Cần Thơ)
- Công nghệ tiết kiệm protein giúp tăng lợi nhuận trong chăn nuôi gia cầm
- Những hạn chế của hàm lượng oxit kẽm trong thức ăn cho lợn con
- Thay thế kháng sinh trong thức ăn cho heo con sơ sinh
- Nhũ hoá chất béo giúp tận dụng tối đa năng lượng khẩu phần
- Protease: Sẵn sàng cho thế giới hậu kháng sinh
- Lịch sử, hiện trạng và xu hướng phát triển của nghề nuôi thú cảnh (PET)
- Cách giảm thiểu tiêu chảy do Rotavirus ở heo con
- Axit Formic: Dùng sao cho đúng và các lựa chọn thay thế
- Tác động của thức ăn côn trùng và vi tảo đến chất lượng thịt gà
- Công nghệ phức hợp miễn dịch và tái tổ hợp trong nhà máy ấp
Tin mới nhất
T4,25/03/2026
- Olmix Asialand Việt Nam tuyển dụng vị trí Quản lý Khách hàng Chiến lược ngành Thú y
- Chế biến sâu – Chìa khóa nâng giá trị xuất khẩu của ngành chăn nuôi
- Kiểm soát chuột: Mắt xích quan trọng trong an toàn sinh học chăn nuôi
- Ứng dụng trí tuệ nhân tạo trong chăn nuôi lợn
- GAIA Việt Nam kỷ niệm 15 năm hành trình kiến tạo giá trị và góp phần định hình tương lai ngành thú cưng
- USMEF: Xuất khẩu thịt lợn của Mỹ tháng 1/2026 tăng cả khối lượng và kim ngạch
- Thị trường thú cưng Việt Nam thu hút doanh nghiệp Hàn Quốc
- Việt Nam sẵn sàng là cầu nối chuyển giao công nghệ phát triển chăn nuôi hiện đại
- Giá sản phẩm chăn nuôi (giá tại trại) cả nước ngày 24/03/2026
- Các xu hướng sẽ định hình ngành TĂCN Hoa Kỳ năm 2026
- AChaupharm: Nấm phổi gia cầm, hiểm họa thầm lặng khi giao mùa
- Chuyên gia bàn giải pháp sử dụng kháng sinh có kiểm soát trong chăn nuôi
- Ngành sữa Việt Nam: Cơ hội “bứt phá” từ nội lực
- Dịch tả heo châu Phi: Hiện trạng và giải pháp kiểm soát hiệu quả (Phần 1)
- Bộ NN&MT mở đợt ‘truy quét’ việc lạm dụng chất kích tăng trưởng, tăng trọng
- Cargill rút khỏi ngành thức ăn thủy sản tại Việt Nam, đóng cửa nhà máy tại Đồng Tháp và Long An
- Chăn nuôi dê bền vững theo chuỗi giá trị: Chủ nhà hàng là mắt xích quan trọng
- Da khỏe, lông đẹp: Chiến lược dinh dưỡng hiệu quả cho heo con sau cai sữa
- Lo ngại bệnh than, Campuchia ngừng nhập một số sản phẩm từ Thái Lan
- Cạn tiền, một công ty tại Nam Phi phải tiêu hủy hơn 350.000 con gà



























































































 đã long trọng tổ chức Hội nghị tổng kết và tri ân khách hàng với chủ đề “Đồng hành dẫn lối tương lai”. Nhân dịp này, Ban Giám đốc công ty đã […]/0.jpg)












Bình luận mới nhất