Chitosan là một biopolymer có nguồn gốc tự nhiên, không độc, được ứng dụng nhiều trong lĩnh vực y sinh học. Đặc biệt, khi làm tá chất cho vaccine, chitosan có hiệu quả trong cảm ứng đặc hiệu kháng nguyên, kích thích miễn dịch tế bào. Việc sử dụng hạt nano chitosan làm tá chất sản xuất vaccine cúm A/H5N1 có giá trị thực tiễn cao, trong điều kiện tình hình dịch cúm A/H5N1 còn tiềm ẩn nhiều nguy cơ, kháng nguyên cúm A/H5N1 kích thích đáp ứng miễn dịch rất thấp trên động vật.
Tình hình sản xuất và tiêu thụ
Việt Nam là một “điểm nóng” của khu vực Đông Nam Á, và là một trong số các quốc gia chịu nhiều thiệt hại nặng nề nhất do virus cúm gia cầm A/H5N1. Chưa đầy một năm sau khi dịch cúm A/H5N1 được ghi nhận ở Việt Nam vào cuối năm 2003, hầu hết các tỉnh thành đều bị dịch tấn công, ít nhất 44 triệu gia cầm bị chết và tiêu hủy, tổng thiệt hại kinh tế ước tính hơn 200 triệu USD.
Nhiều năm qua, đã có nhiều cơ sở, Viện nghiên cứu tại Việt Nam tham gia vào công tác nghiên cứu, thử nghiệm,… các loại vaccin phòng ngừa cúm A/H5N1. Năm 2007, Viện Vaccin Nha Trang đã sản xuất thành công vaccin cúm A/H5N1 trên phôi gà theo qui trình của WHO. Hiện tại công ty Vaccin và Sinh phẩm số 1 đã sản xuất 2 vaccin cúm A/H5N1 trên tế bào thận khỉ tiên phát với hàm lượng kháng nguyên trong 1 liều là 15μg/0.5ml, thử nghiệm lâm sàng giai đoạn 3 cho kết quả bảo vệ khá tốt.
Tuy nhiên, các thử nghiệm bước đầu cho thấy kháng nguyên cúm A/H5N1 cho đáp ứng miễn dịch chưa thực sự cao, chưa đủ để bảo vệ cho con người khi sử dụng các tá chất truyền thống như Al(OH)3 hoặc AlPO4.
Chitosan là một biopolymer của các gốc glucosamine và N-acetyl glucosamine, được sản xuất từ nguyên liệu như vỏ tôm, cua, mực, vách tế bào nấm. Chitosan là một polymer có nguồn gốc tự nhiên, không độc, tương hợp sinh học, phân hủy sinh học và có hoạt tính hấp phụ tốt nhờ tính chất polycation.
Trong lĩnh vực làm tá chất cho vaccin, chitosan có hiệu quả trong cảm ứng DTH đặc hiệu kháng nguyên, kích thích cả tế bào B và T lymphocytes; chitosan có khả năng tăng cường biểu hiện CD 69, tế bào B và CD4+T lymphocytes và tăng cường yếu tố miễn dịch GM-CFS. Do hạt nano chitosan làm tăng hấp thụ, tồn lưu của vaccin trong tế bào miễn dịch, góp phần, cảm ứng mạnh mẽ hệ thống miễn dịch chống lại kháng nguyên. Hạt nano chitosan có khả năng cảm ứng cả hệ thống miễn dịch dịch thể và miễn dịch trung gian tế bào.
Quy trình và phương pháp thực hiện
Hạt nano và micro chitosan được chế tạo bằng hai phương pháp: tạo gel ion kết hợp sấy phun và phương pháp sấy phun trực tiếp.
Qui trình gel ion hóa kết hợp với sấy phun
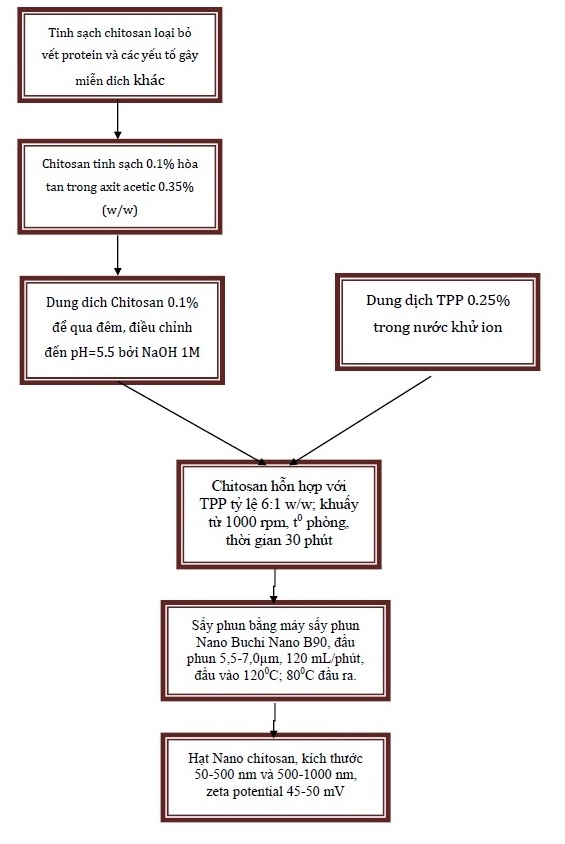
Chuẩn bị nguyên liệu: chitosan được tinh sạch trước khi tạo nano và micro chitosan. Quá trình tinh sạch như sau: bột chitosan được hỗn hợp với NaOH 1M, ủ ở nhiệt độ 60oC trong 2 giờ. Chitosan được lọc, rửa và sấy ở nhiệt độ 40oC trong 12 giờ. Sau khi xử lý NaOH, chitosan được hòa tan trong acid acetic 0.1M và lọc loại bỏ các thành phần không tan. Dung dịch chitosan được kết tủa trở lại với NaOH 1M và thu kết tủa, rửa kết tủa bằng nước khử ion nhiều lần, chitosan được sấy khô chân không trong 24 giờ ở nhiệt độ phòng.
+ Dung dịch chitosan nồng độ 0,025%-0,10% được pha trong acid acetic 0,35%. Hòa tan dung dịch chitosan bằng máy khuấy từ. Sau khi hòa tan, điều chỉnh pH của dung dịch chitosan đến 5,5 bằng NaOH 1M.
+ TPP (Tripolyphosphate) nồng độ 0,25% được pha trong nước khử ion.
Tạo huyền phù nanochitosan:
+ Nhỏ giọt TPP 0.25% vào dung dịch Chitosan 0,025%- 0,10% trong điều kiện khuấy từ; tốc độ 900 vòng/phút; thời gian phản ứng là 60 phút ở nhiệt độ phòng. Tỷ lệ khối lượng chitosan/TPP là 6:1.
+ Thu hồi huyền phù nano chitosan bằng cách quay ly tâm 5.500 vòng/phút trong 15 phút để loại bỏ hết những lắng cặn. Thu hồi dịch nổi chứa nano chitosan.
Sấy phun huyền phù nanochitosan:
+ Dung dịch huyền phù nano chitosan được sấy phun ở nhiệt đầu vào 120oC, nhiệt độ đầu ra 80oC; tốc độ sấy phun 120 mL/giờ; áp suất khí nén 1,2 m3/phút; đường kính đầu phun 4.0μm. Toàn bộ thao tác được thực hiện trong phòng clean bench class two. Mẫu nano chitosan được thu hồi bằng dụng cụ đặc biệt, giữ trong tube thủy tinh vô trùng, nắp vặn. Mẫu được bảo quản ở 5oC trong tủ lạnh.
Sản phẩm nanochitosan thành phẩm ở dạng bột mịn, màu trắng ngà, dạng cầu, đồng đều, bề mặt trơn, kích thước hạt phân bố 50-500 nm và từ 500-1.000 nm. Thế zeta potential hạt zeta potential +45mV đến +50mV. Sản phẩm vô trùng, không nhiễm DNA.
Qui trình thu nhận hạt nano và micro chitosan bằng phương pháp sấy phun
Chuẩn bị nguyên liệu: chitosan được tinh sạch trước khi tạo nano và micro chitosan. Quá trình tinh sạch như sau: bột chitosan được hỗn hợp với NaOH 1M, ủ ở nhiệt độ 60oC trong 2 giờ. Chitosan được lọc, rửa và sấy ở nhiệt độ 40oC trong 12 giờ. Sau khi xử lý NaOH, chitosan được hòa tan trong acid acetic 0.1M và lọc loại bỏ các thành phần không tan. Dung dịch chitosan được kết tủa trở lại với NaOH 1M và thu kết tủa, rửa kết tủa bằng nước khử ion nhiều lần, chitosan được sấy khô chân không trong 24 giờ ở nhiệt độ phòng.
Dung dịch chitosan nồng độ 0,1% được pha trong acid acetic 0,35%. Hòa tan dung dịch chitosan bằng máy khuấy từ. Để qua đêm ở nhiệt độ phòng cho chitosan tan hoàn toàn.
Sấy phun thu hồi hạt: dung dịch chitosan 0,1% có KLPT nhớt từ 276-1200 cPs được sấy phun với nhiệt đầu vào 120oC, nhiệt độ đầu ra 80oC; tốc độ sấy phun 120 mL/giờ; áp suất khí nén 1,2 m3/phút; đường kính đầu phun từ 4,0-7,0μm. Toàn bộ thao tác được thực hiện trong phòng clean bench class two.
Bảo quản đóng gói: mẫu nano chitosan được thu hồi bằng dụng cụ đặc biệt, giữ trong tube thủy tinh vô trùng, nắp vặn. Mẫu được bảo quản ở 5oC trong tủ lạnh.
Sản phẩm nanochitosan dạng bột mịn, màu trắng ngà, dạng cầu, đồng đều, bề mặt trơn, kích thước hạt trung bình 250-1.000 nm; hạt micro 1000-5.000 nm. Thế zeta potential +40mV đến +45mV. Sản phẩm vô trùng, không nhiễm DNA.
Qui trình sản xuất kháng nguyên cúm A/H5N1

Nhân sinh khối: sử dụng tế bào Vero để nhân sinh khối virus được nuôi cấy trong các chai xoay. Khi tế bào phủ khoảng 90% các bề mặt nuôi cấy, tiến hành gây nhiễm virus với liều gây nhiễm 0,001 TCID50/tế bào. Dịch virút được thu hoạch sau 4 ngày nuôi cấy khi các tế bào đã được xâm nhiễm hoàn toàn. Kết quả nuôi cấy được kiểm tra bằng cách xác định hiệu giá ngưng kết hồng cầu HA của vi rút và hiệu giá TCID50 trên tế bào Vero. Các lô nuôi cấy đều đạt hiệu giá HA 512 và hiệu giá TCID50 đạt~109 TCID50/ml.
Bất hoạt và cô lọc kháng nguyên: huyền dịch H5N1 được bất hoạt bằng formalin với tỉ lệ 1/6000 ở 4C có khuấy lắc,48 giờ. Hoạt tính kháng nguyên được kiểm tra bằng phương pháp ngưng kết hồng cầu trước và sau bất hoạt. Cô lọc nhằm loại bỏ những thành phần không mong muốn trong quá trình nuôi cấy, đồng thời cô đặc vi rút với nồng độ cao trước khi tiến hành tinh chế
Tinh chế kháng nguyên H5N1: bằng phương pháp sắc kí lọc gel và phương pháp trao đổi ion âm. Đối với phương pháp sắc kí lọc gel, kháng nguyên được tinh chế trên gel Sepharose 4 Fast Flow, cột XK 16/100 (GE Healthcare). Để đạt hiệu quả cao, thể tích mỗi lần chạy mẫu chỉ chiếm 5% (tương ứng 10 ml) thể tích hạt nêm.
Kháng nguyên tinh chế có độ tinh sạch cao, nồng độ HA bằng kỹ thuật SRID đạt 80μg/ml. DNA tồn dư <10 μg/liều.
Qui trình phối trộn kháng nguyên với tá chất nanochitosan và microchitosan
Quy trình sản xuất vắc xin cúm A/H5N1 hấp phụ hạt nano chitosan
Chuẩn bị kháng nguyên cúm A/H5N1: theo quy trình sản xuất và tinh sạch kháng nguyên H5N1 trên tế bào Vero
Hấp phụ kháng nguyên lên hạt nano chitosan: hạt nano chitosan có kích thước nhỏ hơn 100nm ở dạng đông khô được hoàn nguyên trong dung dịch đệm phosphate (pH 7,2) để đạt nồng độ 2mg/ml. Tiếp tục phối trộn với kháng nguyên cúm A/H5N1 ở các nồng độ kháng nguyên 13,6μgHA/ml và ủ trong 15 phút ở nhiệt độ phòng. Hỗn hợp được ly tâm ở 12.000 vòng/phút, 4oC trong 10 phút và thu dịch nổi để tiến hành đánh giá hiệu quả hấp phụ.
Đánh giá hiệu quả hấp phụ kháng nguyên lên hạt nano chitosan: hiệu quả hấp phụ kháng nguyên lên hạt nano chitosan được xác định bằng phản ứng ngưng kết hồng cầu HA (Hemagglutination assay). Hiệu suất hấp phụ và khả năng hấp phụ của hạt nano chitosan được xác định bằng công thức:
– LE (Loading efficiency) = (Tổng HA – HA dịch nổi)/Tổng HA x 100%
– LC (Loading capacity) = (Tổng HA – HA dịch nổi)/1mg nanochitosan
Phương pháp thực hiện phản ứng ngưng kết hồng cầu HA: dung dịch vi rút được pha loãng bật 2 trong PBS phiến 96 giếng đáy chữ U (50 μl/giếng). Sau đó 50 μl hồng cầu gà 0,5% được bổ sung vào tất cả các giếng, ủ phiến ở nhiệt độ phòng từ 30–60 phút, đọc kết quả. Phản ứng dương tính nếu hồng cầu bị ngưng kết (không tụ ở đáy giếng). Phản ứng âm tính khi hồng cầu không ngưng kết và tụ lại ở đáy giếng. Hiệu giá HA được tính ở độ pha loãng cao nhất của dịch vi rút còn cho phản ứng dương tính. Đơn vị HA được tính bằng cách đảo ngược hiệu giá HA trên một thể tích nhất định. Nồng độ kháng nguyên 13,6μgHA/ml được phối trộn với hạt nano chitosan 2mg/ml cho hiệu suất hấp phụ đạt từ 99%, hiệu giá HA trước khi hấp phụ đạt 20480 HAU.
Quy trình sản xuất vắc xin cúm A/H5N1 hấp phụ hạt micro chitosan
Chuẩn bị kháng nguyên cúm A/H5N1: tương tự như ở quy trình sản xuất vắc xin cúm A/H5N1 hấp phụ lên hạt nano chitosan.
Hấp phụ kháng nguyên lên hạt micro chitosan: hạt micro chitosan có kích thước từ 1.000-3.000nm ở dạng đông khô được hoàn nguyên trong dung dịch đệm phosphate (pH 7,2) để đạt nồng độ 2mg/ml. Tiếp tục phối trộn với kháng nguyên cúm A/H5N1 ở nồng độ 7,5μgHA/ml và ủ trong 15 phút ở nhiệt độ phòng. Hỗn hợp được ly tâm ở 12.000 vòng/phút, 4oC trong 10 phút và thu dịch nổi để tiến hành đánh giá hiệu quả hấp phụ.
Đánh giá hiệu quả hấp phụ kháng nguyên lên hạt micro chitosan: hiệu quả hấp phụ kháng nguyên lên hạt nano chitosan được xác định bằng phản ứng ngưng kết hồng cầu HA (Hemagglutination assay). Hiệu suất hấp phụ và khả năng hấp phụ của hạt nano chitosan được xác định bằng công thức:
– LE (Loading efficiency) = (Tổng HA – HA dịch nổi)/Tổng HA x 100%
– LC (Loading capacity) = (Tổng HA – HA dịch nổi)/1mg nanochitosan
Phương pháp thực hiện phản ứng ngưng kết hồng cầu HA: thực hiện tương tự như ở quy trình đánh giá hiệu quả hấp phụ kháng nguyên lên hạt nano chitosan. Hiệu quả hấp phụ của kháng nguyên cúm A/H5N1 nồng độ 7,5μgHA/ml lên hạt micro chitosan (2mg/ml) đạt xấp xỉ 98%.
Ưu điểm của công nghệ, hiệu quả kinh tế
Qui trình gel ion hóa kết hợp với sấy phun cho phép điều chỉnh kích thước hạt từ 2 khoảng (50-500 nm và từ 500-1.000 nm); phân bố kích thước hạt đồng đều; thế zeta potential lớn 45-50 mV. Phương pháp này có thể thu hồi dễ dàng hạt nano chitosan. Qui trình thu nhận hạt nano và micro chitosan bằng phương pháp sấy phun đơn giản, hiệu suất thu hồi cao.
Ảnh hưởng hiệu ứng kích thước đến tính sinh miễn dịch cho thấy, hạt nano chitosan kích thước nhỏ hơn 1.000nm cho đáp ứng miễn dịch cao hơn so với hạt micro chitosan (1-3μm). Hiệu suất hấp phụ kháng nguyên lên các hạt chitosan kích thước khác nhau đạt trên 95%. Hiệu quả gây đáp ứng miễn dịch của hạt micro chitosan thấp hơn so với hạt nano chitosan. Hiệu suất hấp phụ của các hàm lượng kháng nguyên khác nhau lên hạt nano chitosan đạt trên 97%. Hàm lượng kháng nguyên tối ưu để phối trộn với hạt nano chitosan cho tính sinh miễn dịch cao là 1,5μg/liều, tương tự vậy với hạt micro chitosan là 3μg/liều. Hạt nano chitosan cho hiệu quả cao hơn hạt microchitosan trong cả phát triển vaccine tiêm (tiêm dưới da và tiêm bắp) và vaccine nhỏ mũi.
Vaccine sau khi phối trộn tá chất đạt mọi tiêu chuẩn về tính vô trùng (không có mặt vi khuẩn, nấm, tác nhân ngoại lai), độ pH, nội độc tố, protein tổng số và tính an toàn chung đều đạt tiêu chuẩn theo Dược điển Châu Âu và Việt Nam IV, 2008.
Hạt nano và micro chitosan cũng rất hiệu quả khi sử dụng làm chất mang nano cho thuốc kháng sinh.
Thông tin chuyên gia, hỗ trợ
PGS.TS Nguyễn Anh Dũng
Trường Đại học Tây Nguyên
Địa chỉ: 567 Lê Duẩn, Phường Ea Tam, Thành phố Buôn Ma Thuột, Đắk Lắk.
Điện thoại: 0905426524.
Nguồn: Trung tâm Thông tin và Thống kê KHCN TP.HCM
- InterPet Fest Hà Nội 2026: Cầu nối đưa ngành thú cưng vươn tầm châu Á
- Enzyme protease giúp khẩu phần cao lương rẻ tiền trở nên khả thi
- Sử dụng phụ gia trong thức ăn chăn nuôi: Cần cách tiếp cận khoa học, hài hòa giữa quản lý và thực tiễn
- Ngành chăn nuôi trước xung đột tại Trung Đông: Chủ động xây dựng kịch bản ứng phó
- Sự lên men dạ cỏ
- Hơn 1000 liều vắc xin phòng dại miễn phí được tiêm cho chó, mèo tại Thái Nguyên
- Định hướng nghề nghiệp ngành thú cưng trong kỷ nguyên số
- Công nghệ tiết kiệm protein giúp tăng lợi nhuận trong chăn nuôi gia cầm
- Những hạn chế của hàm lượng oxit kẽm trong thức ăn cho lợn con
- Thay thế kháng sinh trong thức ăn cho heo con sơ sinh
Tin mới nhất
T7,04/04/2026
- Phát triển chăn nuôi đại gia súc tập trung
- Giá thịt cừu Scotland tăng mạnh do nhu cầu cao và nguồn cung toàn cầu khan hiếm
- Chăn nuôi tuần hoàn trên đất cát
- Quy định về trao đổi, chuyển giao kết quả giảm nhẹ phát thải khí nhà kính và tín chỉ các-bon
- Công ty TNHH Muyuan Việt Nam tuyển nhân viên phát triển trang trại chăn nuôi
- InterPet Fest Hà Nội 2026: Cầu nối đưa ngành thú cưng vươn tầm châu Á
- Chi phí đầu vào tăng cao: Ngành chăn nuôi, thủy sản chịu sức ép lớn
- Singapore dỡ bỏ lệnh cấm nhập khẩu huyết heo sau gần 30 năm
- Lâm Đồng tăng cường phòng, chống bệnh dịch tả lợn châu Phi
- Nghiên cứu chọn tạo nguồn chim cút sạch bệnh, rộng đường vào thị trường khó tính
- AChaupharm: Nấm phổi gia cầm, hiểm họa thầm lặng khi giao mùa
- Chuyên gia bàn giải pháp sử dụng kháng sinh có kiểm soát trong chăn nuôi
- Ngành sữa Việt Nam: Cơ hội “bứt phá” từ nội lực
- Dịch tả heo châu Phi: Hiện trạng và giải pháp kiểm soát hiệu quả (Phần 1)
- Bộ NN&MT mở đợt ‘truy quét’ việc lạm dụng chất kích tăng trưởng, tăng trọng
- Cargill rút khỏi ngành thức ăn thủy sản tại Việt Nam, đóng cửa nhà máy tại Đồng Tháp và Long An
- Chăn nuôi dê bền vững theo chuỗi giá trị: Chủ nhà hàng là mắt xích quan trọng
- Da khỏe, lông đẹp: Chiến lược dinh dưỡng hiệu quả cho heo con sau cai sữa
- Lo ngại bệnh than, Campuchia ngừng nhập một số sản phẩm từ Thái Lan
- Cạn tiền, một công ty tại Nam Phi phải tiêu hủy hơn 350.000 con gà




























































































 đã long trọng tổ chức Hội nghị tổng kết và tri ân khách hàng với chủ đề “Đồng hành dẫn lối tương lai”. Nhân dịp này, Ban Giám đốc công ty đã […]/0.jpg)












Bình luận mới nhất